
第43回(令和7年度)
大阪科学賞(OSAKA SCIENCE PRIZE)受賞者の横顔
北島 智也(きたじま ともや) 46歳
現職: 理化学研究所・生命機能科学研究センター
副センター長・チームディレクター
https://chromosegr.riken.jp
略歴:
2001年3月 東京大学理学部生物化学科卒業
2003年3月 東京大学大学院理学系研究科修士課程修了
2004年7月 東京大学分子細胞生物学研究所 助手
2006年2月 東京大学 博士(理学)取得
2007年4月 European Molecular BiologyLaboratory(ドイツ・ハイデルベルク)
博士研究員(日本学術振興会海外特別研究員、HFSP長期フェロー)
2012年1月-現在 理化学研究所発生・再生総合科学研究センター
(現 生命機能科学研究センター)チームリーダー
(現チームディレクター、2019年4月より兼・副センター長)
2012年4月-現在 京都大学大学院生命科学研究科 客員准教授
(2020年4月より客員教授)

研究業績:卵子の老化にともなう染色体数異常の原因解明と抑止技術の開発
卵子は精子と受精することで次世代のすべての細胞の起源となります。親から次世代へ遺伝情報を正しく引き継ぐためには、卵子は正常な数の染色体を持つ必要があります。ところが、ヒトを含む哺乳類の卵子では、染色体数異常の頻度が極めて高く、さらに母体の加齢にともない上昇します。このことは、不妊、流産、そしてダウン症など先天性疾患を持つ出生の原因です。なぜ、次世代にとって重要な細胞である卵子において染色体数異常が頻発してしまうのでしょうか。私たちは、哺乳類モデルとしてマウスを用い、卵子の染色体数異常を引き起こす原因である染色体分配エラーのメカニズムを解明し、その抑止技術を開発しています。これまでに、卵子に特有な細胞特徴と、加齢にともなう欠損の両方が、染色体分配エラーのリスクを高めていることが分かりました。まず、卵子が巨大な細胞質を持つことや、中心体を持たないという特徴が、染色体分配装置である紡錘体の不安定性をもたらし、エラーのリスクを高めることが分かりました。また、老化マウスから得た卵子を生きたまま動画撮影したところ、染色体が早めに分離してしまうことで分配エラーに至ることが分かりました。さらに、これらのエラーを抑止するために、細胞内で紡錘体と染色体の動きを操作するマイクロマシンとして人工動原体を開発しました。この人工動原体は老化マウス卵子の中で紡錘体に自律的に働きかけ、染色体の早期分離を妨げて、染色体数異常を抑えることが分かりました。この研究は、生命のはじまりの細胞である卵子における染色体分配機構の不完全性の謎を解く手がかりになるとともに、不妊治療などで用いられる生殖補助技術に貢献する可能性があります。
第43回大阪科学賞 記念講演
卵子の老化の原因解明と抑止技術の開発
国立研究開発法人理化学研究所 生命機能科学研究センター
副センター長・チームディレクター
北島 智也はじめに
卵子は女性の生殖細胞である卵母細胞からつくられる配偶子で、精子と受精して次世代のすべての細胞の起源となります。したがって、卵子は次世代へ生をつなぐための「はじまりの細胞」と呼べます。卵子を介して母から子へと遺伝情報を伝える担い手となるのが、DNAを含む構造体である染色体です。ヒトでは1番から22番までの22種類の常染色体と、XとYの2種類の性染色体があります。もし、卵子が異常な数の染色体を持つと、それは不妊、流産、先天性疾患(ダウン症など)の原因となります。卵子は他の細胞に比べて染色体数異常になりやすく、さらに母体の加齢とともにその頻度が上昇します。この現象はよく「卵子の老化」とも表現され、不妊治療における大きな壁ともなっています。なぜ、次世代へ生をつなぐ「はじまりの細胞」としての役割を担う卵子で、染色体数異常が起こりやすいのでしょうか。
私たちの研究室では、卵子の染色体数異常の原因を解明し、さらにはそれを抑止する技術を開発するための基礎研究を行っています。卵子の染色体数を決定するのは、一段階前の細胞である卵母細胞における染色体分配です。卵母細胞は減数分裂と呼ばれる特別な様式の細胞分裂を行い、娘細胞として生まれる卵子に染色体を分配します。卵子が染色体数異常となるのは、この際の染色体分配にエラーが起こるためです。では、卵子をつくるための染色体分配で、特に母体が加齢したときに、エラーが起きやすいのはなぜでしょうか。
1.老化卵子では染色体の早期分離を経てエラーが起こる
私たちはそれを解明するために、ヒトと同じ哺乳類であるマウスをモデルに実験を行いました。加齢させた老化マウスから卵母細胞を取り出し、顕微鏡下で生きたまま培養して卵子へと成熟させることで、染色体が分配エラーに至るまでの動きを完全追跡できる動画を得ることに世界で初めて成功しました。その動画には、染色体分配エラーの原因イベントが記録されていました。正確な染色体分配は、分配の瞬間に一本の染色体が二本に分離することで達成されます。ところが、老化した卵母細胞では、染色体分配よりずっと早いタイミングで一本の染色体が二本に分離してしまっていました(図1)。これを早期分離と呼びます。これら早期分離した染色体が、数異常となって卵子へと分配されていました。この観察から、染色体の早期分離が、老化卵子における染色体数異常の原因であると考えられました。

図1:老化マウス卵子における染色体の早期分離。染色体(赤)と動原体(緑)の顕微鏡画像。矢頭は早期分離して二つに分かれた染色体を示す。
2.染色体分配装置の内側はエラーの原因を引き起こす危険地帯
次に、どのような染色体が、どのような機序で早期分離するのかを調べました。そのために、生きたマウス卵子内の染色体の番号を顕微鏡下で特定しながら追跡できる技術を開発しました。さまざまな番号の染色体の追跡結果を大量に取得してビッグデータとし、それをもとに定量解析を行ったところ、小さいサイズの染色体は染色体分配装置である紡錘体の赤道面の内側へ、大きいサイズの染色体は外側へと配置されやすいことが分かりました。どうやら、内側と外側では違いがありそうです。では、分配エラーの原因である染色体の早期分離はどこで起きるのでしょうか?調べると、ほとんどの早期分離が内側で起きていました(図2)。ということは、小さいサイズの染色体ほど内側へ動きやすく、そこで早期分離して分配エラーになりやすいということです。これらの観察結果から、染色体分配装置の内側は染色体にとって危険地帯であり、そこに配置されることが、分配エラーの原因である早期分離のリスクを高めると考えられました。
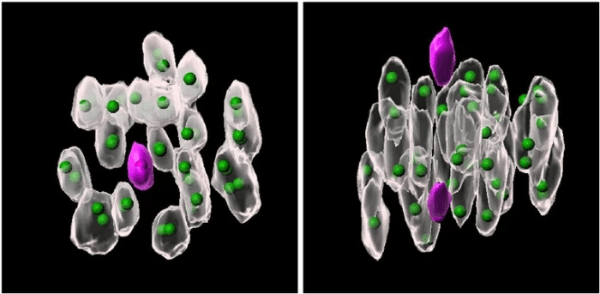
図2:染色体の早期分離は内側で起こる。染色体(灰色)の配置を上から(左図)と横から(右図)見ている。
早期分離した染色体を紫色で色付けしている。緑の球は動原体の位置。
3.人工動原体で染色体を危険地帯から逃がすことで卵子エラーを抑止する戦略
もし、この仮説が正しければ、染色体の内側への動きを妨げることで、分配エラーを抑止できるはずです。でも、どうやって染色体の動きを操作できるでしょうか。そのために、染色体がどうやって動いているかを考えてみます。染色体は自身の動きを操縦する運転席を持っています。それが動原体です。動原体は、染色体のセントロメアとよばれる領域に形成される分子複合体で、染色体分配装置と接続して染色体を動かします。そこで私たちは、卵子の中に新たな運転席として人工動原体をつくることで、染色体の動きを変化させることを発想しました。人工動原体は、生きたマウス卵母細胞の中に微小ビーズを注入し、その表面に動原体タンパク質を付着させることで作成されました。この人工動原体ビーズは自律的に染色体分配装置と接続し、染色体のように動ける性能を持ったマイクロマシンです。興味深いことに、この人工動原体ビーズは、染色体にとって危険地帯である染色体分配装置の内側に自ら身代わりとなって入っていき、染色体がそこに配置されないよう防いでくれる能力を持っていました(図3)。まさに、私たちが欲しいと願っていた性能です。そこで、老化マウスの卵母細胞に人工動原体ビーズを入れてみました。すると、染色体分配エラーの原因である染色体の早期分離が抑えられることが分かりました。私たちの仮説と一致する結果です。それと同時に、老化卵子の染色体数異常を抑止するための技術開発へ向けた道がついに拓かれました。
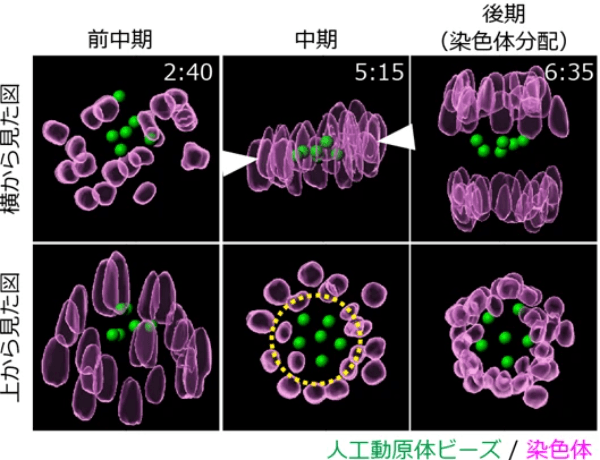
図3:卵子内で人工動原体ビーズは染色体の内側配置を防ぐ。人工動原体ビーズ(緑)と染色体(紫)を示す。
横から見た図で、中期において染色体と同様にビーズが整列していることが分かる(白矢頭)。
これを上から見ると、人工動原体ビーズは内側領域(黄色点線)を占領し、染色体がそこに入らないよう防ぐことが分かる。
4.まとめ
この研究を開始した13年前、私は卵子の老化を抑止するのは不可能ではないかと思っていました。卵子の染色体数異常の原因を解明できたとしても、その原因を修正するのは無理筋であることを示すことになるだろうと予期していたのです。原因が染色体の早期分離であることが分かった時点で、その思いはさらに強まったものです。ところが、研究室メンバーの地道な努力と幸運な偶然も重なり、卵子の染色体数異常を抑止する技術開発への道筋が拓けました。可能性が0だったものを1にするのは基礎研究の醍醐味です。今では私は、卵子の老化は抑止可能であり、人類が生殖補助技術に活用する未来はいずれ来るだろうと思っています。でも正しく活用するためには、何が必要でしょうか。それはもしかしたら、私がこの研究を開始するきっかけとなった、まだ解けていない疑問と関係するのかもしれません。なぜ、世代をつなぐ「はじまりの細胞」である卵子がエラーを起こしやすく、不完全にできているように見えるのか。そこには意味があるのでしょうか、ないのでしょうか。答えがあるのかも分かりませんが、それを追求せずにはいられません。
用 語 集
染色体
遺伝情報の運び手で、DNAとそれに結合するタンパク質などの分子で構成されます。ヒト女性の細胞は通常、22種類の常染色体と1種類の性染色体(X染色体)を二本ずつ持ち、そのうち一本は母から、もう一本は父から受け継いだものです。男性の細胞は、同様に22種類の常染色体を2本ずつに加え、性染色体として父から受け継いだ1本のY染色体と、母から受け継いだ1本のX染色体を持ちます。
卵子と精子
卵子と精子は配偶子と呼ばれる細胞で、有性生殖を担います。卵子は卵巣内で卵母細胞という生殖細胞からつくられます。その際には減数分裂という特別な細胞分裂が行われ、卵子に染色体が分配されます。卵子が精子と融合することで受精卵となり、次世代のすべての細胞の起源となります。
染色体分配
細胞は分裂する際、DNA複製されてできた染色体コピーを娘細胞へ均等に分配し、同一の染色体セットを持たせます。卵子や精子をつくるために生殖細胞が行う減数分裂においては、母と父から受け継がれた染色体どうしが組み換えられたあと、卵子や精子に染色体が分配されます。
染色体分配装置、動原体
染色体分配のための細胞内装置は紡錘体と呼ばれます。紡錘体の主要な構成因子の一つは、チューブリンというタンパク質が糸状に重合した微小管です。多くの動物細胞は中心体を二つ持ち、それらは紡錘体の両極に位置して微小管重合を担います。微小管は、染色体それぞれが持つ動原体のペアに接続します。動原体はセントロメアと呼ばれるDNA領域と100種類以上のタンパク質を含む巨大複合体で、微小管と接続して染色体の動きを制御する能力を持っています。微小管は動原体ペアに接続すると、それらを紡錘体の両極に向けて引っ張ります。これが、染色体を分配するための牽引力となります。卵子は中心体が無いため、他の細胞とは異なる機構を用いて紡錘体を形成すると考えられます。
先天性疾患、ダウン症
先天性疾患とは、生まれながらにして持つ疾患です。ダウン症は先天性疾患の一つで、通常は細胞あたり2本の21番染色体が、生まれつき3本あることで引き起こされます。この状態は21番トリソミーと呼ばれます。過剰な21番染色体は卵子由来であることが多く、それは卵子がつくられる際の染色体分配エラーによる数異常に起因します。母体の加齢にともない、次世代のダウン症の頻度が上昇します。
生殖補助技術
生殖を成立させるために用いられる技術で、体外受精や顕微授精などの技術を含みます。もともとは畜産などの分野で動物生産のために発展した技術で、今では不妊治療に応用されています。不妊治療のための技術として生殖補助医療とも呼ばれます。体外受精による生殖補助医療への貢献により、ロバート・エドワーズ氏に2010年ノーベル医学生理学賞が贈られました。
Q&A
記念講演の際にいただきました質問に対して、北島先生にご回答いただきました。
<研究のきっかけ・姿勢・考え>
①このテーマについて研究しようと思ったきっかけを教えて下さい。
②研究活動を行う際に、生命機能科学研究センターに行き着いた理由をお聞きしたいです。
⇒
①と②はまとめて答えます。大学院生のときに分子遺伝学を学び、分裂酵母を用いて減数分裂の染色体分配を研究していました。当時から、卵母細胞の染色体分配エラーは重要問題として分野内で認識されていました。博士号取得後、哺乳類の研究に移りたいと思い、研究員としてドイツに留学し、マウス卵母細胞のライブイメージング技術を学びました。その技術を論文発表したころ、それを用いれば卵母細胞の染色体分配エラー研究が独自のアプローチでできると気づきました。理研の生命機能科学研究センターは、若手の研究者をリーダーとして研究室立ち上げを手厚くサポートしてくれる研究機関で、いろんな世代の卓越した研究者が揃っています。そのような環境で研究室リーダーとして研究してみたいと思いました。
③私は高校1年生で、SEEDSプログラムや高校の活動で、高校生の内に研究の大会等で大きな成果を上げることを目的に励んでいます。先生は13年も前から研究を続けられているとお聞きしたのですが、いち高校生が短い期間で大きな成果を得るために何が大切でしょうか。
⇒
③まず興味のある問題を見つけてください。その問題を解くために、必要があれば仮説を立て(仮説なしで徹底観察でも構いません)、他の誰もやっていないアプローチを考案してください。データが出たら、できるだけ批判的にデータを解釈して考察してください。データから示されたこと、示唆されること、残された問題を区別して整理してください。なお、研究において成果は結果であって目的ではありません。
④マウスでの実験に成功されましたが、人体でも先生の技術を用いた実験をすることは予定されていますか。また、この研究には段階ごとにどの程度の期間を費やし、何人程度のチームで役割分担をして進められましたか。私自身ドイツでの研究に興味があり、EMBLで研究されることになった経緯やそこでの研究内容についてもお伺いしたいです。
⇒
④私自身はヒト卵母細胞を用いた研究は今のところ予定していませんが、将来的には可能性はあります。この研究を開始した当時は5人ほどのチームで始めて、今は15人ほどに増えています。メンバー各自は異なるテーマで研究しつつ、大きな方向性は研究室として一体になるようにしています。ドイツEMBLで研究した経緯と内容は、①で回答します。
⑤研究を進める時に、特に苦労した部分はどこですか。
⇒
⑤家庭(特に子育て)との両立です。妻をはじめ家族には感謝しています。
<研究手法・技術開発・異分野連携>
⑥講演レジュメの中で、「生きたマウス卵子内の染色体の番号を顕微鏡下で特定しながら追跡できる技術」を開発されたとありましたが、生物学を研究されている研究者の方々自身が、研究を進めるために他の分野の技術開発に励まれることがあるのでしょうか。
⇒
⑥それが必須と言ってもよいくらいです。分野内にある既存の技術、手法、視点だけでは新しい研究の可能性が大幅に限られます。私自身、他の研究分野からの情報を常に勉強し、人材を取り入れるようにしています。分野を超えることで研究の独自性を高めることができます。
⑦人工動原体の設計コンセプトに興味があります。天然のものをモデルに人工で作ることには限界があると思います。その設計プロセスについてご教示いただけますと幸いです。(どこを諦めてどこを作りこんだかなど)
⇒
⑦私たちの人工動原体の設計コンセプトは、天然の模倣に拘っておらず、むしろ天然と異なる設計から尖った特性を持たせるアプローチです。人工動原体ビーズは、ビーズ表面に限られたタンパク質を付けただけなので、天然とは全然似ておらず、細胞内で機能するという予想はありませんでした。ただ、誰もやったことが無く面白そうだったからやってみたら、細胞内で機能するという予想外の結果が得られました。大事なのは予想して作り込むことだけではなく、誰もやったことがないことをやることだと思っています。
⑧ご講義の中で「現在は人工動原体にタンパク質を用いている」とありましたが、タンパク質以外の物質を用いたときとタンパク質を用いたときの働きの違いがあれば、教えていただきたいです。また、染色体の早期分離について、哺乳類に特有とのことですが、哺乳類の中でも寿命の長さの違いによって、早期分離の起こりやすさの違いがあるのか、また、マウス以外でも人工動原体の働きは変わらないのか、お答えいただけると幸いです。
⇒
⑧今のところ、ビーズもしくはタンパク質粒子を土台にした人工動原体をつくりました。ビーズのほうが大きく、そのおかげで一つあたりの微小管接続量は多いです。一方、タンパク質粒子は細胞内で大量に生成されるので、全体としての効果は大きいです。哺乳類の中で寿命の長さと染色体早期分離の起こりやすさに関係があるかは、大変興味深い問題です。まだはっきりとしていません。寿命をヒトは約100年、マウスは約2年と単純に考えてみると、マウス卵子の染色体数異常が10%を超えるのは1.5歳くらいです。ヒト卵子では33歳ころに50%を超えます。これをどう解釈するかは、視点によると思います。より多くの哺乳類でのデータも必要と思います。
⑨この技術を実際に医療の現場で使うためにはどんなことが必要ですか。また、最初に制作されたビーズの人工動原体と、最後にご紹介していただいたタンパク質の人工動原体の違いは何ですか。
⇒
⑨この技術により老化マウス卵子の染色体数異常が抑えられることが分かりましたが、その卵子から次世代の産仔が得られるかの検証が必要です。また、この技術は卵母細胞から卵子に成熟培養させるときに介入する技術ですが、医療の現場でも成熟培養させる技術がより確立される必要があります。ビーズとタンパク質の人工動原体の違いは、⑧で説明します。
⑩本質から離れた質問かもしれませんが、発表スライドの人工動原体の有無と染色体分配におけるエラーの割合との関係を示すグラフの上部に記載された0.01963(あいまい)という数字はどのような意味があるのでしょうか。
⇒
⑩統計学的な有意性の指標となるp値と呼ばれるものです。例えばコントロール群と実験群に差があると言えそうか、というときに統計学的な計算をして、p値が小さいほど有意な差がありそうだと言えます。ご興味があれば「統計」「p値」などで検索して調べてみてください。
<開発された人工動原体の仕組み・作用・設計・量>
⑪染色体への早期分離の対処法として、人工動原体をつくることを行っていましたが、ほかの微小管などの部分ではなく動原体に着目したのですか。私はこの講義を聞くなかで、年齢とともに微小管も衰えていくと思い、その点を用いてもよいのではないかと思っています。
⇒
⑪ご指摘のとおり、動原体ではなく微小管をターゲットにして操作する発想もできると思います。実際、そのような研究も今行っているところです。年齢とともに微小管が衰えていくという指摘も、幾つかの研究ではあります。
⑫人工動原体ビーズの量が多すぎた場合、染色体が引っ張られないということは起こりますか。また、人によって微小管の数が異なるなどがあれば、調整が必要になりますか。(ビーズの量について)
⇒
⑫ご指摘のとおり、人工動原体が多すぎると、染色体が引っ張られなくなって、染色体分配自体がうまく行かなくなってしまいます。人工動原体は適切量でないと良い結果を得られません。人によってその量が異なる、あるいは同じ人でも卵母細胞によって異なる、ということは十分考えられると思います。自身で効果を調節できるスマートな人工動原体を設計できると良いかもしれません。
⑬先天性異常の仕組みについては学びますが、その原因となるプロセスについて、今回初めて知り、非常に興味を持つことができました。今回の講義の中で、人工動原体ビーズが微小管と多く結びつき、コヒーシンへとかかる力を和らげる、ということはないのでしょうか。また、ビーズを注入する量などは、どのように決めるのでしょうか。
⇒
⑬ ⑫の質問と共通するところが多いので、そちらもご覧ください。ご指摘の通り、人工動原体が微小管と結びついたことで、天然の染色体が微小管に引っ張られる力が弱まり、したがってコヒーシンに掛かる力が和らいだと思っています。実験では、人工動原体を注入する量は、染色体の動きを過度に邪魔しない、という指標で決めました。
⑭人工動原体ビーズは、染色体のおとりとなって、微小管と結びつくというお話でした。染色体に結びつく微小管が不足し、正常に染色体の分離が行われなくなる、ということはないのですか。
⇒
⑭ご指摘のとおりです。⑫でお答えします。
⑮自分が特に気になったのは、コヒーシンを扱うのが難しいとありましたが、コヒーシンをコピーして「わっか」を二重にすることは難しいのでしょうか。また、分離することを一時的に止めるように染色体が1つに集ったタイミングに動原体を周りで囲むように配置することはできないのでしょうか。
⇒
⑮コヒーシンを新たに合成して輪っかをつくることはできると思います。ただ、その輪っかを染色体ペアを留めるように狙って閉じるのが、今の技術では難しいです。天然のコヒーシンの閉じ方を模倣するのではなく、新たな設計で狙って閉じれる人工コヒーシンを作れば良いかもしれません。
⑯人工動原体ビーズを人間の卵子に注入するとなると、人工物が胎児の中に残ってしまうと思うのですが、それがなんらかの悪影響を及ぼす可能性はありますか。
⇒
⑯あると思います。そのため、ビーズではなく自然分解が期待できるタンパク質粒子を土台とする人工動原体のほうが比較的安心と思っています。
⑰「人工動原体ビーズ導入卵子」について、染色体を正常に分離できた後、その卵細胞や個体における遺伝子異常の頻度は通常レベルでしょうか。個体発生は通常通り進むと考えられますか。
⇒
⑰ ⑯、⑱でビーズが分解されないという懸念について答えます。一方、タンパク質粒子を土台とする人工動原体は自然分解されますが、その後の影響については、今後検証すべき重要な課題です。今の知見をもとに考えれば、染色体数を正常にすれば、個体発生は通常通り進むと予想されます。ただ、誰もやったことがありませんので、そこに予想外の発見がある可能性もあると思っています。
⑱未解明な部分であったら申し訳ないのですが、染色体が分配する際に残った人工動原体ビーズは細胞に何かしらの影響を及ぼすことはないのかということが気になりました。
⇒
⑱ビーズは分解されずに残ってしまうので、何かしらの影響を及ぼす可能性が排除されることはないと思います。
⑲卵子に入る人工動原体ビーズやその代替としてのタンパク質がお話に挙がっていましたが、その入れ込みによって卵子に悪影響はないのでしょうか。また、異常な物体として排除されることはないのですか。
⇒
⑲ ⑯~⑱で答えます。異常な物体として積極的に排除されることは、現時点では予想されませんが、可能性はあります。
⑳人工動原体ビーズは、身代わりになった後はどのようになるのですか。
⇒
⑳ ⑯~⑱で答えます。
㉑人工動原体が染色体分配装置の内側に入ることで染色体異常を防げるのであれば、わざと染色体分配装置の外側に人工動原体がくるようにすれば、染色体異常を起こりやすくできるのか、また、その際の問題点と役立つ点を教えていただけると幸いです。
⇒
㉑人工動原体を外側に来るようにすれば、卵子の染色体数異常が起こりやすくなる可能性はあると思います。実は、がん細胞では外側の染色体ほど数異常になりやすいことが報告されていて、卵子とは逆です。外側でおとりになる人工動原体ができたとしたら、がん細胞の染色体数異常を抑止するツールの発展に貢献するかもしれません。
<倫理・安全性・医療応用・社会的影響>
㉒マウスでの実験に成功されましたが、マウスや人体に影響を及ぼす実験において研究倫理にかかわる課題にはどのように対処された・する予定でしょうか。
⇒
㉒動物実験実施に関わる法令、所内規程を遵守し、それらに基づく動物実験申請・審査や毎年の講習の受講などを行っています。ヒト卵子を用いる実験についても国・学会・所内での規定があり、倫理委員会の承認のもとで研究を行います。
㉓人工動原体の研究を生殖補助に活用できるようになるとおしゃっていましたが、もし将来応用できるようになったとして、何年後での実現になるのか、また、何歳までが限度になるのか、お考えをお聞きしたいです。
⇒
㉓老化卵子の染色体数異常を抑止する技術だけなら、10年後に使われるようになっていても私は驚きません。何歳までが限度になるかは、⑰で答えたことを含め検証が足りていませんので、現時点では考えることが難しいです。
㉔人間に応用していくとなると、どのタイミングでどうやって、人工動原体を注入していくことになりますか。
⇒
㉔今回の人工動原体を応用することを考えるならば、卵巣を穿刺して卵母細胞を取り出した後に、人工動原体の材料を顕微注射で注入することが想定されます。その後、卵子へ成熟培養させる必要があります。⑨に関連した回答があります。
㉕卵子の老化を遅らせる技術の確立によって、女性や男性のライフプランにどのような影響が出ると考えていますか。
⇒
㉕妊娠や子育ての期間を考慮したライフプラン・キャリアプランについて柔軟性が高まると思います。
㉖卵子の老化が完全に防げるようになったとき、倫理的・社会的にはどんな課題が生まれるとお考えでしょうか。また、「卵子があえて不完全であることに意味があるかもしれない」というお話が印象的でした。先生ご自身は、この“不完全さ”にどんな生命の意義を感じていますか。さらには、人工動原体によって“危険地帯”から染色体を逃がすというアプローチは非常に革新的ですが、この手法が実際のヒト卵子に応用されるためには、どのような課題が残っているのでしょうか。
㉗実際に女性の卵子の老化の抑制が普及するための課題などがあれば教えていただきたいです。
⇒
㉖と㉗はまとめて答えます。老化の卵子を防ぐことによる影響は、すぐに次世代に出るものではなく、世代を重ねることで出る可能性もあります。これをヒトにおいて検証することは現実的にはできません。同様の懸念は、すでに用いられている生殖補助技術でも、完全に払拭されているわけではありません。それでも、現在の社会では一定の理解のもとで用いることが容認されています。応用の可否のラインをどのように設定するかは、生命科学のみならず、社会的・倫理的な議論が必要です。卵母細胞の染色体分配が不完全に見えることは、生殖が多様性を生むことと少なからず関係があるのではないかと私は感じていますが、根拠があるわけではありません。不完全に見えることに意味はないという可能性も十分あります。ただ、それを知りたい動機としては、生命がそもそも不完全であることを理解することで、いろんなことに寛容になれるのではないかという気持ちはあります。ヒト卵子への応用に向けた課題については、⑯⑰⑱㉓㉔などの他の回答で答えます。
<卵子・哺乳類の生物学的特性・加齢の影響>
㉘マウスの卵子の研究で得られた染色体分配エラーなどの原因、人間の卵子にも同様に当てはまるのですか。人間の卵子の研究は難しいように考えます。マウスの実験だけでは起きないが、人間の卵子ではおきうるエラーなどの反応はどのように実験するのですか。
⇒
㉘今回の研究で明らかにした染色体の早期分離は、ヒト卵母細胞でも見られます。ヒト卵母細胞・卵子を用いる研究は、不妊治療において得られた卵母細胞・卵子の中から、治療に用いられず廃棄予定となったものについて、提供者の同意と倫理委員会の承認のもと、研究に使用されることがあります。ただ、マウスのほうが卵母細胞・卵子のほうが数・質ともに研究に使いやすく、ヒト卵母細胞・卵子の研究が比較的難しいのはご指摘のとおりです。㉙哺乳類の卵子において、染色体数異常の頻度が極めて高く、さらに母体の加齢にともない上昇するという現象は、なぜ起こると思われますか。現段階の仮説を簡潔に教えてください。
⇒
㉙ ㉖の答えに含めます。
㉚講義後の2つ目の質問の答えに、20年前に作られた卵母細胞が使われているとのことでしたが、マウスなどは寿命が短く人間のように20年も老化することはないと思います。ネズミの卵細胞は人間のそれよりも早く老化、劣化するのですか。
⇒
㉚ ⑧の答えに含めます。
㉛人間の細胞やサルの細胞を用いるのではなく、ネズミの細胞を用いて実験をどうして行われているのですか。また、どのような違いがヒト卵子とあると考えられていますか。
⇒
㉛ ㉘の答えにも含めます。霊長類であるサルの細胞を用いることは、よりヒトに近いモデルとして有効です。ネズミはサルより短い期間で多くの産仔が得られること、小柄で扱いやすく飼育がより省スペースでよいことなど、研究面での利点があります。私たちのマウスを用いた研究からは、染色体の早期分離が卵子の染色体数異常の主要な原因でした。ヒト卵子の異常の原因は、それだけではなく他の原因もあることが指摘されています。その研究のためには、霊長類モデルを用いることが必要になるかもしれません。
㉜今回は哺乳類の卵子についての研究をされていましたが、魚類や鳥類でも同じような結果が得られるのでしょうか。
⇒
㉜今回紹介した卵母細胞の老化は、卵母細胞が胎児期のみにつくられて長期間維持されるという哺乳類の特徴と関係していると考えています。成体で卵母細胞をつくることができる魚類は、哺乳類のような卵母細胞の老化とは異なると考えられます。鳥類については私は答えられるだけの知識がありません。
㉝なぜ哺乳類は染色体異常がおきやすいのでしょうか。また、卵生と胎生との違いが影響するとしたら、人間も卵生にすることは不可能でしょうか。
⇒
㉝ ㉜に答えを含めます。哺乳類が胎生であることと関係はあると思います。人間を卵生にすることは、卵子の染色体数異常を止めることよりも遥かに難しいことは間違いありません。
<染色体の分配・エラー・分子機構の仕組み>
㉞先生が講義中におっしゃっていた「生物のメカニズムの不完全性」に関して、私個人の意見として「DNAという大方安定で遺伝を行える遺伝子を得た弊害として分配の際のエラーを生み出すことになった」と考えています。先生はどのようにこの問いに対して考えていらっしゃいますか。
⇒
㉞興味深い視点だと思います。DNAは長期的な安定性を持った分子ですので、遺伝情報の維持に向いています。一方で、種の維持のためには多様性を生むことが重要であり、そのために有性生殖が進化したと思われます。多様性を実現する延長としてエラーを生み出すことになった、という仮説はあり得ると思います。
㉟「はじまりの細胞」である卵子がエラーを起こしやすい理由について、現在、どのようなお考えをお持ちですか。
⇒㉟ ㉖の答えに含めます。㉞も関連します。
㊱減数分裂時にエラーが起きると、流産やダウン症につながるとおっしゃられていましたが、特定のエラーが起こると決まった症状がでるものなのかご教授お願いします。
⇒㊱21番染色体過剰(トリソミー)がダウン症、18番トリソミーがエドワーズ症、X染色体不足(Xモノソミー)がターナー症、X染色体過剰(XXY)のクラインフェルター症などがあります。それぞれの症状は異なります。
㊲精子の染色体分配で、染色体数異常になるケースは今までありましたか。また、起こる可能性があるのか。コヒーシンの交換は前例がないとのことだが、今後できると思いますか。
⇒㊲精子の染色体数異常もありますが、卵子と比べてずっと少ないです。その代わり精子では、高齢になるほど変異が多くなります。コヒーシンの交換は難しいと私は思いますが、⑮で答えるような人工コヒーシンを用いる戦略はあり得ると思います。
㊳先天性疾患の原因が精子側にある事例はあるのでしょうか。
⇒㊳ ㊲で答えを含めます。精子で高齢になるほど蓄積する変異は、次世代でのがんや自閉症のリスクと関連することが指摘されています。
㊴微小管のはたらきが弱まりすぎて分裂できなくなる、ということはあるのでしょうか。
⇒㊴あります。⑪や⑫で答えます。
㊵なぜ、染色体が分裂する際に①わっか②とめぐ③ひも④はさみの段階をふむようになったのか、それは生命の進化のどの段階で身に着けたものなのか教えていただけると嬉しいです。
⇒㊵進化を考えるうえで解けていない重要な問題の一つです。真核生物の多くは①~④の道具を用いる原理で染色体を分配しますので、真核生物の原始的な段階で獲得したと思われます。DNAを凝縮する道具、DNAとタンパク質をつなぐ道具、移動や輸送用のひも状の道具、タンパク質を分解する道具は原核生物も有しており、おそらくこれらが①~④の道具として転用されて進化したものと考えられます。
大阪科学賞 運営委員会事務局




